Värma vatten - Testexperiment
Laboranter: Isabelle, Shilma & Louise
Laboranter: Isabelle, Shilma & Louise
Inledning
En bestämd massa vatten ska värmas till en viss temperatur, och tiden detta kommer att ta har förutsagts med hjälp av sambandet:
E (energi i kJ) = P (effekt i kJ/s) · t (tid i sekunder) = m (massa i kg) · c (konstant) · ΔT (temperaturförändring i ºC), med den tidigare laborationens C-konstant.
Först testas en temperaturförändring på 10 ºC, sen 20 ºC.
E (energi i kJ) = P (effekt i kJ/s) · t (tid i sekunder) = m (massa i kg) · c (konstant) · ΔT (temperaturförändring i ºC), med den tidigare laborationens C-konstant.
Först testas en temperaturförändring på 10 ºC, sen 20 ºC.
För testerna är massan och och energitillförseln förutbestämd och konstanta.
Massan är 0,3 kg vatten, uppmätning av denna mängd vatten sker direkt i termosen.
Samma doppvärmare med effekten 300 W skall användas.
Massan är 0,3 kg vatten, uppmätning av denna mängd vatten sker direkt i termosen.
Samma doppvärmare med effekten 300 W skall användas.
Hypotes
Hypotesen är att c = 4,33 kJ/(kg · ºC)
Förutsägelse
Om C-konstanten sätts som 4,33 kJ/(kg · ºC) ger det att:
E = m (massa)· c (konstant)· ΔT (temperaturförändring)
E = m · 4,33 kJ/(kg · ºC) · ΔT
Doppvärmarens effekt är 300W
E = m · 4,33 kJ/(kg · ºC) · ΔT
Doppvärmarens effekt är 300W
Då antas att sambandet att E = m· c· ΔT gäller för uppvärming av vatten, och att C-konstanten är samma oavsett start- och slut-temperatur på vattnet.
Två temperatursförändring (ΔT ) skall testas; 10 ºC och 20 ºC .
Test 1: ΔT = 10 ºC
E1 = 300 W · t1 = 0,3 kg · 4,33 kJ/(kg · ºC) · 10 ºC,
E1 = 300 W · t1 = 12.99 kJ
t1 = 43 sekunder
Sluttemperaturen ska bli 10ºC mer än starttemperaturen
t1 = 43 sekunder
Sluttemperaturen ska bli 10ºC mer än starttemperaturen
Test 2: ΔT = 20 ºC
E2 = 300 W · t2 = 0,3 kg · 4,33 kJ/(kg · ºC) · 20 ºC,
E2 = 300 W · t2 = 0,3 kg · 4,33 kJ/(kg · ºC) · 20 ºC,
E2 = 300 W · t2 = 25,98 kJ
t2 = 87 sekunder
Sluttemperaturen ska bli 20ºC mer är starttemperaturen.
t2 = 87 sekunder
Sluttemperaturen ska bli 20ºC mer är starttemperaturen.
Metod
300 gram vatten mättes upp i en termos. Temperatursstickan och doppvärmaren placerades i termosen. Starttemperaturen noterades. Då doppvärmarens kontakt kopplades in i uttaget, startades tidtagaruren. Under förloppet rördes vattnet om genomgående i måttlig hastighet. Efter att vattnet nått sin sluttemperatur stoppades tidtagningen, och tidsförloppet noterades samt jämfördes med den förberäknade tiden.
Nytt vatten användes efter varje test.
Nytt vatten användes efter varje test.
Uppställningen av materiel: våg, termometer, termos med vatten, doppmätare.
Inte med på bild: Tidtagarur
Resultat
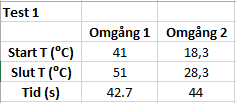
Test 1: Temperatursskillnad 10ºC
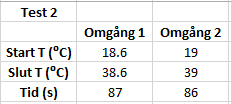
Test 2: temperatursskillnad 20ºC
Diskussion
För test 1 hade tiden förutberäknats till 43 hela sekunder, och resultat blev 42,7 och 44 sekunder.
För test 2 hade tiden förutberäknats till 87 hela sekunder, och resultat blev 87 och 86 sekunder.
Testets värde låg mycket nära förutsägelsens värden och detta visar att den var korrekt.
Detta innebär att vår hypotes c = 4,33 kJ/(kg · ºC) stämmer, då förutsägelsen var baserad på denna. Resultatet visar att vattnets specifika värmekapacietet är 4,33 kJ/(kg · ºC) för denna laboration, eftersom utfallet resulterade med det som hade förutsagts.
Testets värde låg mycket nära förutsägelsens värden och detta visar att den var korrekt.
Detta innebär att vår hypotes c = 4,33 kJ/(kg · ºC) stämmer, då förutsägelsen var baserad på denna. Resultatet visar att vattnets specifika värmekapacietet är 4,33 kJ/(kg · ºC) för denna laboration, eftersom utfallet resulterade med det som hade förutsagts.
Dessutom stärks antagandet att C-konstanten gäller oavsett temperatur på vattnet och definieras som “den mängd energi som behövs för att höja 1 kg vatten med 1ºC”, eftersom testet utfördes med olika starttemperatur och med olika temperatursintervall. Utfallet resulterade med det som hade förutsagts och antagits.
Eventuella felkällor är noggrannheten på C-konstanten det vill säga stokastiska felkällor, vilket beror på felkällor från tidigare labben, samt ytterligare energiförluster från doppvärmaren. Men eftersom samma sorts doppvärmare användes blev energiförlusterna under observationslaborationen och denna testexperiment näst intill identiska, och det är troligen därför C-konstanten gav en passande förutsägelse.
Dock kan värdet på C fortfarande vara för högt i teorin och för andra, effektivare uppvärmningsmetoder. Därför är ytterligare en felkälla att samma metod för energitillförsel användes, och C-värdet skulle kunnat bli mer tillförlitligt med annat uppvärmingsinstrument.
Vattnets specifika värmekapacitet gäller för allt vatten i universum. Det ger att allt vatten behöver 4,33 kJ (universalt; 4,18 kJ), per kg vatten, för att molekylerna ska få mer inre rörelseenergi och sedan bryta de intermolekylära bindningarna. Detta är alltså en omvandling av energin som tillförts enligt termodynamikens första huvudsats, “energi kan endast omvandlas mellan olika former och inte skapas/förstöras”.
Vatten har en hög specifik värmekapacitet jämför med andra ämnen. Det innebär att det värms upp långsamt men även kyls ner långsamt.
Detta kan märkas på till exempel sjöar. En sjö kan vara mycket kallare än luften, till exempel en ovanligt varm vårdag. Det beror är för att vattnet behöver lång tid (eller en stor del energi, som kan ges under lång tid) att värmas upp på grund av sin höga värmekapacitet, och sjön kan därför vara kylig långt in på sommaren.
Likaså kan en sjö vara varm även fast det är kallt ute, och fryser först sent in på vintern.
Detta kan märkas på till exempel sjöar. En sjö kan vara mycket kallare än luften, till exempel en ovanligt varm vårdag. Det beror är för att vattnet behöver lång tid (eller en stor del energi, som kan ges under lång tid) att värmas upp på grund av sin höga värmekapacitet, och sjön kan därför vara kylig långt in på sommaren.
Likaså kan en sjö vara varm även fast det är kallt ute, och fryser först sent in på vintern.
Ett annat exempel på hur vattnets höga specifika värmekapacitet kan märkas av i vardagen, är när en pizza konsumeras. Det högst möjligt att tomaten bränner tungan. Tomat, som innehåller omkring 95% vatten, värms upp långsamt i ugnen men kommer sedan också svalna långsamt. När den resterande pizzan svalnat till lagom ätbar temperatur kommer tomaten fortfarande vara brännhet. På grund av att luft har sämre värmeledningsförmåga, så kommer tomaten, som har en högre mängd energi, att ta längre tid för att svalna. Därför bränns tungan.
Slutsats
Förutsägelsen stämde överens med hypotesen och har därför stärkts. C - konstanten/vattnets specifika värmekapacitet är 4,33 kJ/(kg · ºC) för vatten i flytande tillstånd och för denna metod.
Inga kommentarer:
Skicka en kommentar